TOPICS【共創事例】国立がん研究センター・帝人・J-TEC・HUグループ・三井不動産が仕掛ける柏の葉再生医療プラットフォーム~国立がん研究センター・先端医療開発センター センター長土井先生/J-TEC畠社長
SCROLL

- 国立研究開発法人 国立がん研究センター
- 一般社団法人UDCKタウンマネジメント
- 三井不動産株式会社
- H.U.グループホールディングス株式会社
- 株式会社ジャパン・ティッシュエンジニアリング
- 帝人株式会社

日本の医薬品産業の柱の一つとして期待される再生細胞等製品。これまでの低分子医薬品や抗体薬などのバイオ医薬品とは違った製品開発のノウハウが求められます。特に医療機関でのヒトの組織を採取するところから製品作りが始まり、疾患や個々の患者ごとに性質の違う細胞を増やすため、レギュレーションを熟知したうえで、製造に高度なノウハウが求められます。
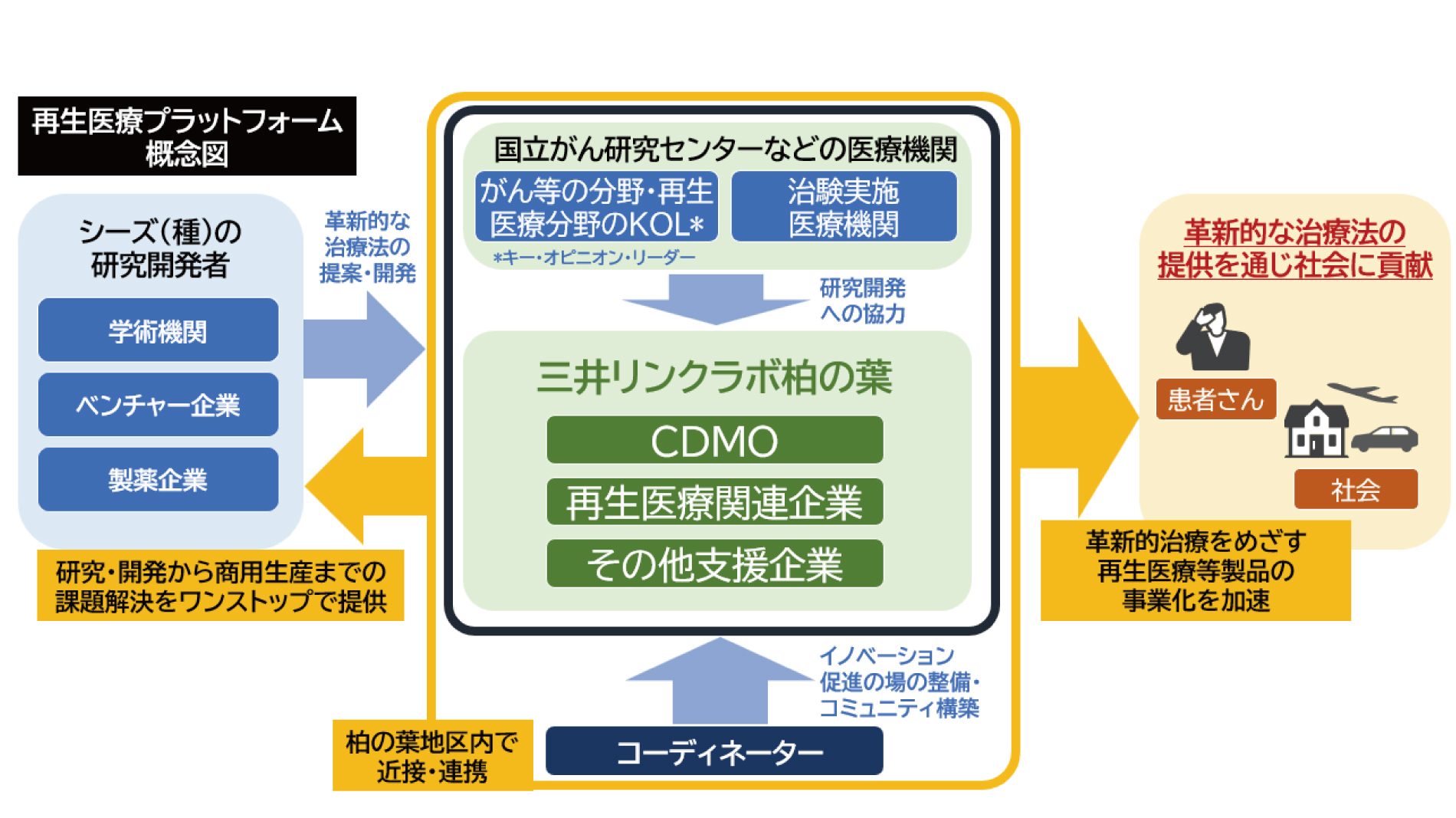
柏の葉では、日本でCAR-Tの治験を主導してきた国立がん研究センター東病院と再生細胞等製品の製品開発に実績を持つ帝人・ジャパン・ティッシュエンジニアリング(J-TEC)、HUグループ、場とコミュニティー形成に実績のある三井不動産がタッグを組み、2022年秋に『柏の葉再生医療プラットフォーム』を立ち上げました。(問い合わせ先、一般社団法人UDCKタウンマネジメント E-Mail : rmpf@udcktm.or.jp)
このプラットフォーム設立をリードした国立がん研究センター・先端医療開発センター(NCC・EPOC)センター長の土井先生、J-TECの畠社長に、日本の再生細胞医療の課題点、今後の展望について語っていただきました。
[Abbreviation]
CAR-T ; キメラ抗原受容体T細胞 (Chimeric antigen receptor T cell). ADC ; 抗体-薬物複合体 (Antibody-Drug Conjugate). GLP ; Good Laboratory Practice(医薬品の安全性に関する非臨床試験の実施の基準に関する省令). GMP ; Good Manufacturing Practice(医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令). CDMO ; Contract Development and Manufacturing Organization(医薬品開発製造受託機関)
再生細胞医療との出会い
―まずお二人にこれまでのご経歴と現在のお仕事についてお尋ねします。
土井:私はもともと肝臓内科医で、細胞傷害性リンパ球のCD8+T細胞などの機能を研究していました。その中にはPD-1やサイトカイン、細胞接着分子等もあり、当時の研究が最近になってようやくがんの治療に使われるようになってきています。一方、臨床では内視鏡を専門にしていて、がんの初期治療に用いられるESD(内視鏡的粘膜下剥離術)における止血鉗子を考案し、製品化した経験もあります。こうしたモノづくりへの関心が高じて薬というモノの臨床開発に関わるようになったのです。2022年には、国立がん研究センターで先端医療開発センター(EPOC)と橋渡し研究推進センター(CPOT)のセンター長に就任し、現在、アカデミアの先生たちを中心とした固形癌をターゲットとする再生細胞医薬品の第Ⅰ相試験チームのお手伝いをしています。がんの細胞治療に関わり始めたのは、現在がんの再生細胞医療の先端を走っているアカデミアの先生方から再生細胞医薬品の第Ⅰ相臨床試験が国内ではできないということを言われて、協力するようになりました。当時国内では細胞免疫療法に関する知見が少なく、どれくらい効くのか、どのような副作用が出るのか経験がありませんでした。一方でCarl H. June先生ら海外の著名な先生たちから、「臨床で非常によく効く」という情報が流れてきました。ただし、70%以上の症例でサイトカイン放出症候群(CRS)の副作用が出て集中治療室(ICU)で管理しないといけないということもあり、各施設での受け入れが難しかったのだと思います。そのような中で、中面先生をはじめ、がんセンターとして第I相臨床治験チームとしてお手伝いを始めました。それが噂を呼んでアカデミアの先生方が自分たちの研究しているCAR-Tをがんセンターに持ち込み始めました。
がんの再生細胞治療法(免疫細胞療法)は、ドライバー遺伝子(がんを引き起こす遺伝子)陽性の限られた患者さんを対象とするがんゲノム医療に比べ、がん抗原タンパクのように遺伝子ではなくタンパク質レベルをターゲットとするため、多くのがん患者さんたちに治療を届けることができます。また、一人ひとりの患者さんに合った治療を私たちはオーダーメードと言わずにカスタム化と言っています。まず共通のプラットフォームを作りあげ、いろんな中身をユーザーの好みに合わせて作る。バイオ医薬品の一番いいところは、個々の技術プラットフォーム、例えば抗体-薬物複合体(ADC)にしてみても、再生細胞医薬品にしても、あるいは今後出てくるメッセンジャーRNAワクチンにしてみても、患者さんに合った治療が出来てくるので、多くの方たちに届けることができるというメリットもあります。
畠:私は歯科医として、地元の渥美半島で、歯科医院を開業しようと思っていた人間です。ところが、名古屋大学大学院時代に教授から口腔粘膜細胞の培養というテーマを与えられ、ティッシュエンジニアリング領域に関心をもつようになりました。1999年に大学発ベンチャー企業を日本に1,000社作るという目標がミレニアム・プロジェクトで掲げられ、ジャパン・ティッシュエンジニアリング(J-TEC)が創業しました。名古屋大学の人間としてお手伝いをしていた私は2004年にJ-TECに入社し、再生医療との付き合いが本格的にスタートします。創業当初は、再生医療の事業、研究・開発、申請・承認、製造・販売といった機能をすべて担う必要があったため、試行錯誤の連続でした。そうこうしているうちに日本に「再生医療産業」を作り、ゆくゆくは「再生医療文化」を構築することに貢献したいと考えるようになったわけです。ただはじめは、こういう形で企業人になるとはゆめゆめ思ってもいませんでしたね。
再生医療等製品の開発では、「高級車」より普及しやすい「大衆車」を目指すべき
―わが国の再生医療の現状と課題について、どのようにお考えになっていますか。
畠:2013年11月の薬事法改正に伴い、「再生医療等製品」という新たなカテゴリーが作られ、それに伴う条件及び期限付承認制度も導入されました。このことは、わが国の再生医療の発展に大きな流れを作り、現在17品目が再生医療等医薬品の承認を受けています(2023年2月現在)。日本はこれまで「細胞を用いた組織再生」の開発が盛んでしたが、近年は、CAR-T細胞療法に代表される遺伝子治療や細胞治療が海外で積極的に開発され、再生医療の多様性が明らかになってきました。逆にみれば、多くの人たちが再生医療に「夢の医療」という期待感を抱きながらも、その目指すゴール、用いる原料など、取り組む人たちによって表現の仕方が異なり、概念が明確化されないまま研究開発がバラバラに進んできたと言うこともできます。現在、治療に結びつくシーズも生まれてきている中で、それをどう社会実装していくかが問われていると思います。
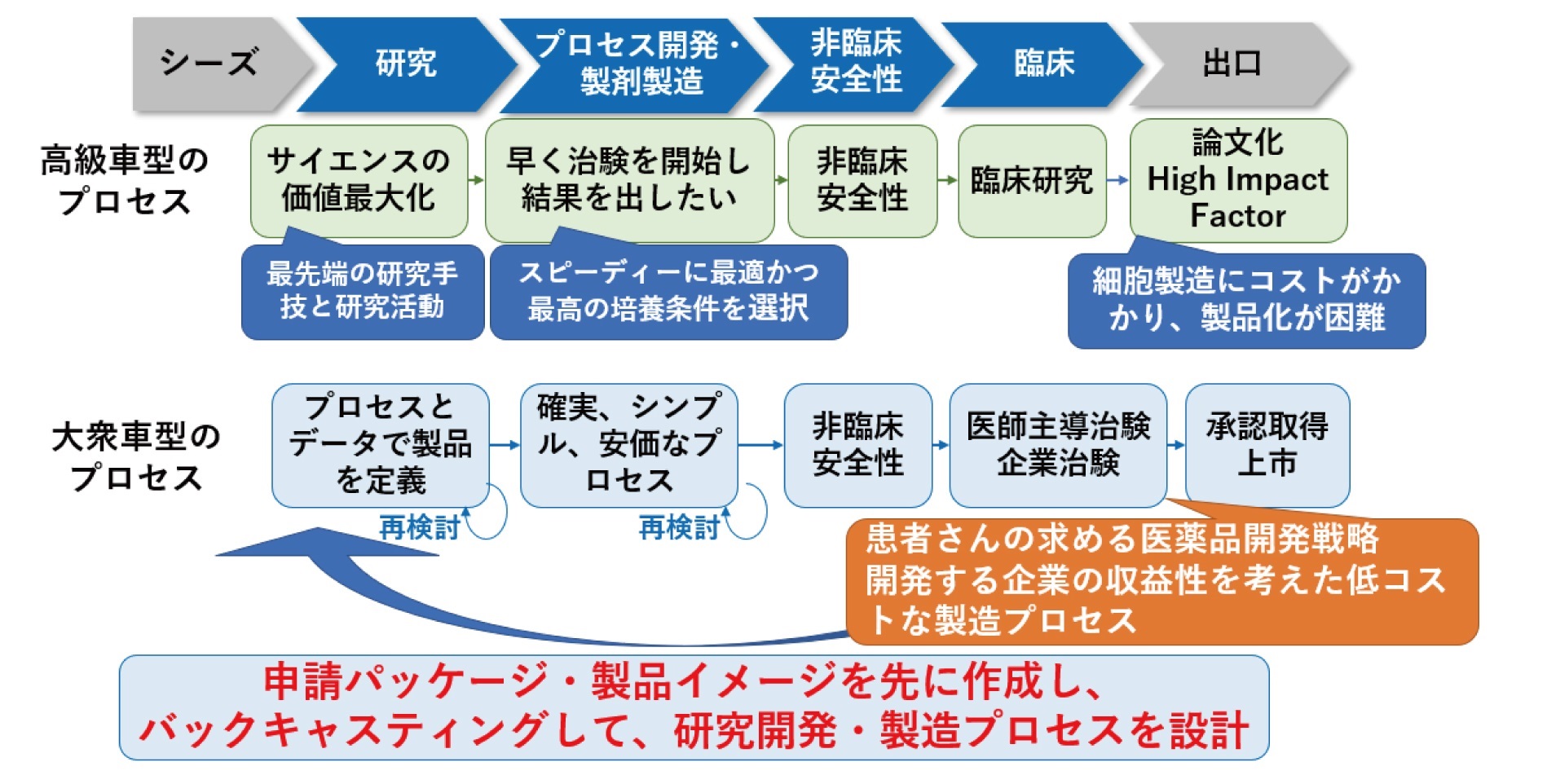
土井:私は2つの課題があると思います。1つは、臨床試験をできる環境の整った病院が日本にはほとんどないこと。再生医療等製品が従来の医薬品や医療機器とはまったく概念が違うものだということです。企業から病院に完成品が届き、使用する医薬品や医療機器に比べ、再生医療等製品は、例えば原料の細胞採取は病院で行い、それを企業に渡して加工した後に再び病院に戻され、患者さんに用いられます。すると院内でのサンプルの扱う工程がGLPやGMPに準拠したものでなければならず、原料の採取から院内の輸送に至る工程の中では、細胞の品質保証は病院側の人間が行わなければならない。その概念がこれまでの日本の病院にはなく、そういった臨床試験の経験も皆無でした。海外でCAR-T細胞療法などの再生細胞医薬品の開発がいち早く進んだのは、そのような臨床研究のシステムが整っていたからです。二つ目は、日本では製造販売をあまり意識せず開発を進めてきたことかと思います。海外では、実験室レベルから始まる様々な工程において、その品質を保証する規格化されたプラットフォームを研究者とCDMO企業が共に作り上げてきました。一方、日本のアカデミアの研究者は自身の研究室でのやり方に固執するあまりCDMO側との意思疎通があまり図られてこなかったという構図があります。論文投稿時に高評価を得たいため、研究者は最高の材料、最高の条件の下で結果を出そうとします。しかし、その条件をCDMO企業が忠実に再現して大量生産につなげることは難しいのです。これを私は「限定生産される高性能高級車」と「広く普及している大衆車」の比喩でよく説明します。数千万もするような高級車は最高の性能を持ちますが、大量生産できません。一般公道を走るだけなら、大量生産できる大衆車で十分です。多くの患者さんに再生医療等製品を届けるという意味で、医薬品研究に関わる者は普及しやすい大衆車のようなものを目指すべきだと思います。
畠:まさにその通りですね。私たちは、それぞれの再生医療等製品を社会実装できる合理的な手法を確立することを「製品の作り込み」と表現しています。その中で大切なのは、アカデミアの先生方とCDMO企業との「合意形成」です。研究開発から事業化までの障壁を「魔の川」、「死の谷」、「ダーウィンの海」と呼びますが、製品化から事業化までに横たわる「ダーウィンの海」を越えることで、初めて多くの患者さんに再生医療の恩恵が届きます。製品の作り込みは、この最終目標を踏まえた逆算的なアプローチ、いわゆるバックキャスティングの考え方で行わなければなりません。こうした考え方をCDMO企業は医療機関の先生方と、単なるユーザー・サプライの関係ではなく、胸襟を開いて議論できる場を作るべきであり、またそうした人材を育成する努力を怠ってはならないでしょう。
創薬開発・事業化の加速を促す新たなプラットフォーム構築を目指す
―柏の葉を拠点とした「再生医療プラットフォーム」が2022年秋に立ち上がりました。発案者の一人である土井先生にその背景を紹介いただければと思います。
土井:シカゴ大学は院内に大きなオープンラボ(アカデミアラボ)を設置しています。近隣施設の研究者の製造プロセスを受託する創薬プラットフォームが機能し、いくつもの臨床試験が行われ、新たな製品が生まれています。ここでは、Douglas Bishop博士が作られたSOP(標準作業手順書)をすべての製造プロセスで遵守するというルールがあり、どのプロジェクトも同じ品質が保証されています。国立がん研究センター(NCC)でも、アカデミアの研究者からがんの再生細胞治療開発の相談が寄せられており、東病院で過去に製造施設を作れないか検討したことがありましたが、限られた予算の中で、実際に再生細胞を提供できる患者さんは年間数十人程度しか見込めませんでした。そこで、シカゴ大学のようなプラットフォームを日本で作れないものかと三井不動産の方に相談したところ、柏の葉に新たな研究棟(三井リンクラボ柏の葉1)を建設予定でそこにCDMO企業を誘致したらどうかとなりました。そこで海外展開も視野に入れてCDMO企業にも参加を仰ぐことで、研究・開発から事業化まで一貫してプロジェクトを推進できる新しい「再生医療プラットフォーム」の構想に発展したのです。SOPを作るノウハウは既にNCCもある程度持っていましたが、CDMO企業の参加で、新たな再生医療開発拠点ができることを期待しています。
畠:柏の葉再生医療プラットフォームは再生医療等製品開発のモデルケースになる可能性があると考えています。日本における再生医療の発展にまつわる問題点について、開発事業者である企業と医療機関の先生方が胸襟を開いて話ができることはとても重要です。新しいイノベーション構築のための課題解決に向けた取り組みができる環境になることを期待しています。ここで再生医療等製品の開発・事業化という1つの成功事例が生まれるなら、それは全国の他の拠点でも応用・展開できる医療研究開発モデル、社会実装モデルになるでしょう。まさに目的志向型のプラットフォームになってもらいたいと思っています。これに加えて、海外展開できる日本発の再生医療等製品を作ることも今後の大きな課題です。そのゴールをアカデミアの先生方とCDMO企業が共有できる場になってほしいものです。
柏の葉スマートシティから全国へ、再生医療をムーブメントに
~アカデミアと企業の新たなパートナシップから生み出されるイノベーションへ~
――最後に今後の再生医療発展に向けた抱負についておうかがいします。
畠:日本の再生医療環境は必ずしも楽観視できる状態ではありません。資金面、人材面、モダリティなど、課題は山積しています。わが国の再生医療発展において最初に着手すべきは、やはりアカデミアの先生方と企業側の方々とのさまざまな合意形成だと思っています。また、こうした議論をする前提として、多様な再生医療領域を適切に整理することが必要になるでしょう。その上でとにかく成功事例を生み出し、人材を育成する。海外展開については、海外からのインバウンドをどう集めるか、海外への導出方法、出ていく先は欧米なのかアジアなのかなど、テーマはいくつもありますが、まずは同じ土俵で議論をスタートさせることが大切です。
日本発の再生医療等製品を海外に展開するにはやはりモノの製造の合理化、機械化、それからその経験を基にした製品品質の作り込みにあると思っています。いかに社会実装に適した製品の仕様を決定するのか。これには、品質の標準化という考えも必要かもしれません。実際の製品提供経験をもとにした細胞培養工程の機械化や合理化、言い換えれば、再生医療等製品製造のパッケージ化を実現していくべきです。こういった一連の流れができれば、いっそう海外進出しやすくなるのではないでしょうか。先ほどの土井先生の大衆車の話にあったように、普及させていく仕組みづくりが日本のものづくりの強みではないかと思います。柏の葉再生医療プラットフォームはこうした一連の活動を有機的につなげる仕組みにしたいですね。
土井:日本の再生医療は、「均てん化」から「集約化」へと考え方を変える時期にきていると思います。例えば海外では、ある治療ができる拠点病院が地域に1つと限定されているため、必然的に患者さんはその施設に集まってきて、資金が動き、開発も進みます。日本のがん医療の均てん化政策は、日本で再生医療の技術のプラットフォームを広げていく上では障害になっていましたが、今回の再生医療プラットフォームの試みはそれを越えていくものだと位置づけています。いち早く再生細胞医薬品を患者さんに届けるというゴールは、研究者もCDMO企業も同じです。いろんな立場の人たちや企業が柏の葉スマートシティに集まり、産業団体である再生医療イノベーションフォーラム(FIRM)や国とも連携しながら、研究開発から事業化までを一気に加速させる。そこで得られたノウハウを全国に広げることで、新たな拠点を作る。この柏の葉から日本に再生医療のムーブメントを起こしていければと思っています。
製法の最適化・高品質かつ低コストでの細胞の供給・臨床現場との連携による再生細胞医療等製品の研究開発加速化を担う『柏の葉再生医療プラットフォーム』。日本の製造業の強みである製品品質の造り込み・製造のパッケージ化をもとに再生細胞医療を日本の強みとして実現できる可能性を聞かせていただきました。今後ますますの発展が期待されます。
詳しいお問い合わせは以下まで。
一般社団法人UDCKタウンマネジメント E-Mail : rmpf@udcktm.or.jp
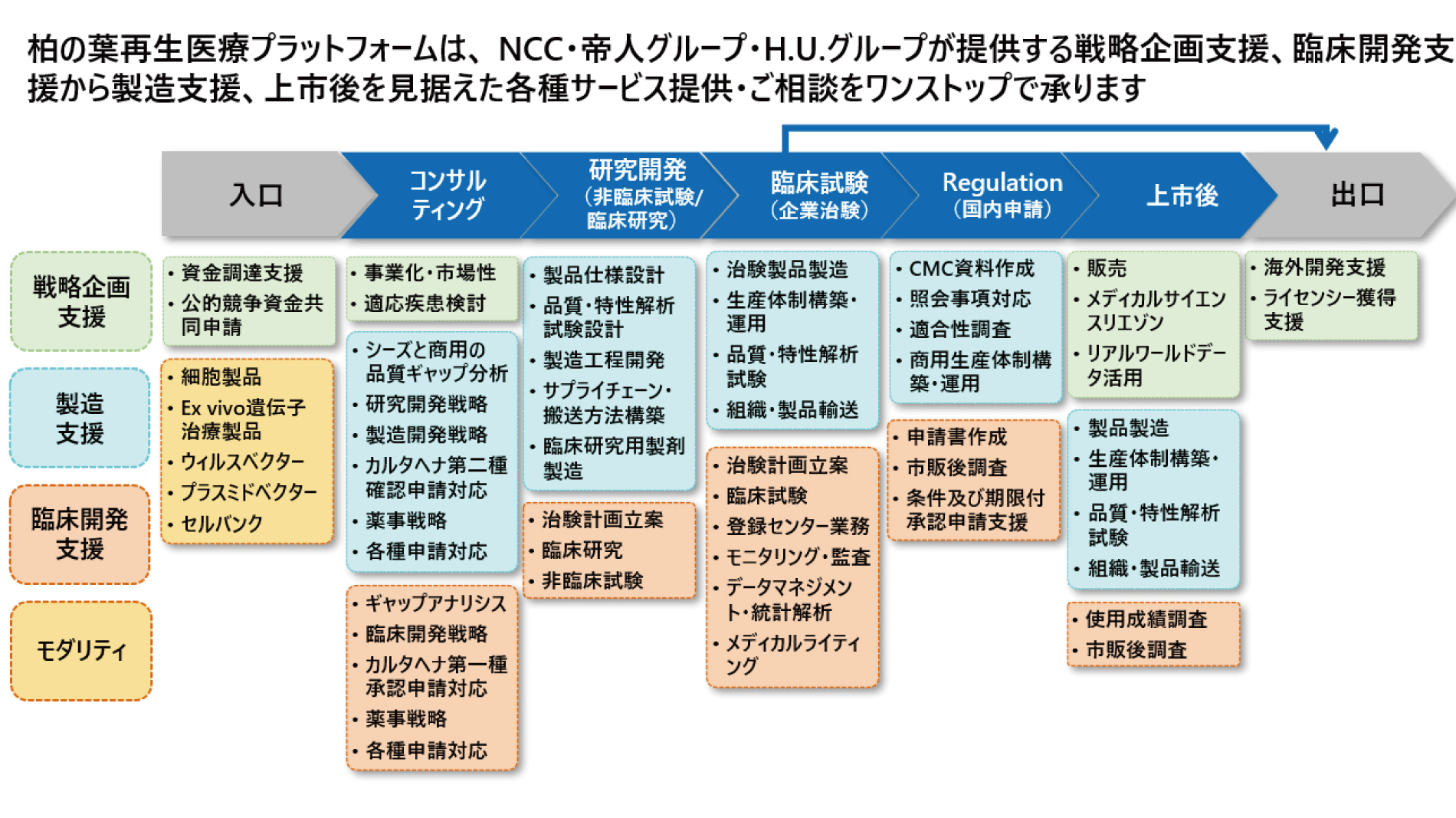
図3 柏の葉再生医療プラットフォームが提供するサービス

畠 賢一郎 氏
株式会社ジャパン・ティッシュエンジニアリング 代表取締役 社長執行役員
1991年広島大学歯学部卒業、歯科医師免許取得後、1995年名古屋大学大学院医学研究科博士課程修了、同年名古屋大学医学部附属病院歯科口腔外科医員、2002年名古屋大学医学部附属病院遺伝子・再生医療センター助教授を経て、2004年(株)ジャパン・ティッシュエンジニアリング(J-TEC)入社、取締役研究開発部長、2017年富士フイルム再生医療事業部長兼RD統括本部再生医療研究所長、J-TEC代表取締役社長執行役員。2019年より再生医療イノベーションフォーラム(FIRM)会長に就任。再生医療領域における産学連携を積極的に推進する役割を担っている。

土井 俊彦氏
国立がん研究センター 先端医療開発センター(EPOC) センター長 、橋渡し研究推進センター(CPOT) センター長、東病院先端医療科長
1989年岡山大学医学部卒業。1994年岡山大学大学院医学研究科第一内科修了、国立病院四国がんセンター内科勤務。2002年国立がんセンター東病院内視鏡部へ転任。2013年早期・探索臨床研究センター先端医療科長/東病院消化管内科長を経て2014年より副院長(研究担当)。2015年から東病院先端医療科長。2022年先端医療開発センター長兼橋渡し研究推進センター長に就任。早期臨床開発、特に第Ⅰ相臨床試験を実施。新薬、新規医療技術に加え最近は、再生医療・細胞医療、バイオマーカー探索や画像解析、また、AI・IoT を利用したDXへの取り組みなどを介して基礎から臨床導入・開発を強力に推進することを目指す。
PAGE TOP













